前回は、水槽立ち上げ初期の最大の壁である「アンモニアの毒性」について解説しました。
今回は、そのアンモニアが硝化(酸化)されることで生じる「亜硝酸(亜硝酸塩)」の毒性について深掘りしていきます。
淡水のシュリンプ水槽など甲殻類を中心に飼育している水槽では特に恐れられる亜硝酸ですが、淡水水槽と海水水槽、そしてサンゴ水槽では、その危険メカニズムが少し異なることをご存じでしょうか?
本記事では、アンモニアと同様に「淡水と海水で毒性がどう変化するのか」、そして生体が死に至るメカニズムと、もしもの時の対処法について、詳しく解説します。
亜硝酸(HNO₂)と亜硝酸イオン(NO₂⁻)の違い
アンモニアがろ過バクテリア(ニトロソモナス等)によって酸化されると生成されるのが、第2の毒「亜硝酸」です。亜硝酸もまた、水槽のpH(水素イオン濃度)によって、その形態と毒性の強さを変える性質を持っています。
亜硝酸(HNO₂):毒性が極めて強い
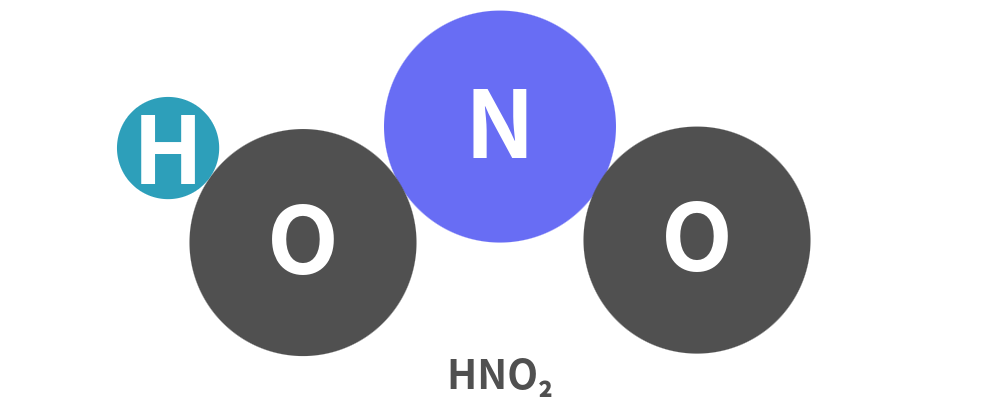
酸性環境(pH6以下)で増える形態。
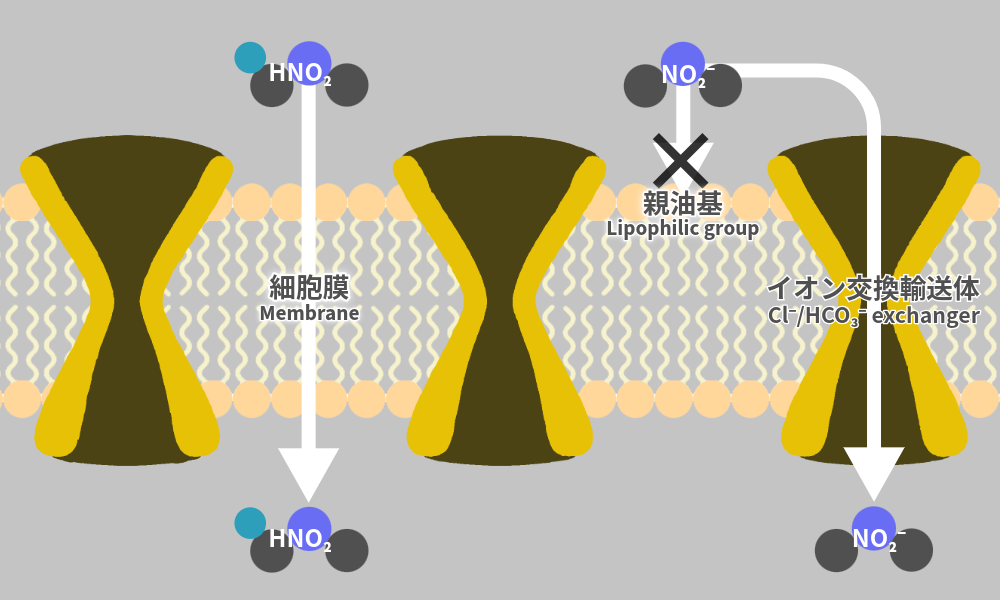
脂溶性(油に溶けやすい性質)を併せ持ち、生体の細胞膜を直接通り抜けて侵入する「強毒タイプ」です。
▶酸性・中性の水中での挙動(pH6以下)
水中には水素イオン(H⁺)が豊富にあります。
亜硝酸イオン(NO₂⁻)はH⁺を受け取り、毒性の高い「亜硝酸(HNO₂)」へと姿を変え、その量が急増します。NO₂⁻ + H⁺ → HNO₂
亜硝酸イオン(NO₂⁻):条件次第で猛毒になる
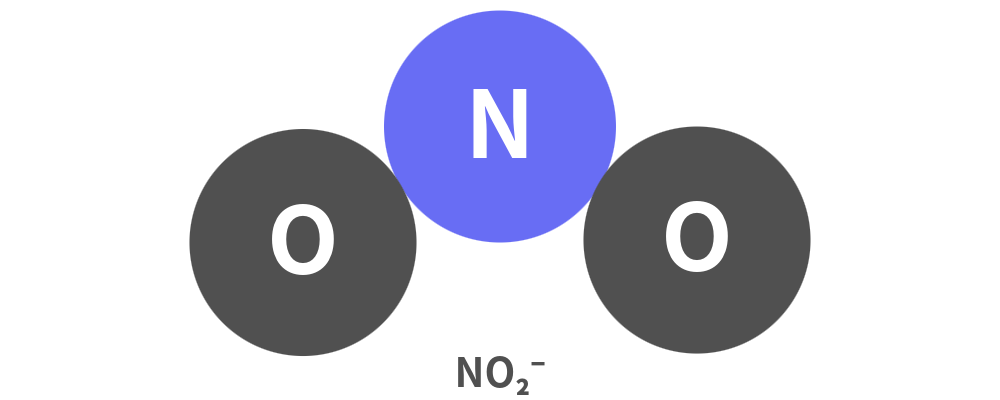
電荷を持ち親水性(水に溶けやすい性質)のため、基本的には細胞膜を通過しにくい形態です。
一般的なアクアリウム環境(pH6.5~8.4)では、亜硝酸のほとんどがこの状態で存在しています。
▶中性付近の弱酸性~アルカリ性の水中での挙動(pH6.5以上)
pHが上がるほど水中にはH⁺が少なくなります。
すると、亜硝酸(HNO₂)からH⁺が離れ、亜硝酸イオン(NO₂⁻)の割合が増えます。HNO₂ - H⁺ → NO₂⁻
pH8以上の海水環境などでは、OH⁻(水酸化物イオン)が増えるため、強毒のHNO₂はほとんど水中から消えてしまいます。
HNO₂ + OH⁻ → NO₂⁻ + H₂O
pH低下に伴う「強毒化」のリスク ※淡水水槽の場合
「うちは淡水だけどpHは中性だから大丈夫」と思っていても、油断は禁物です。
以下のグラフをご覧ください。これはpHの変化によって、亜硝酸が「強毒(HNO₂)」と「イオン(NO₂⁻)」のどちらの形態で存在するかの割合を示したものです。
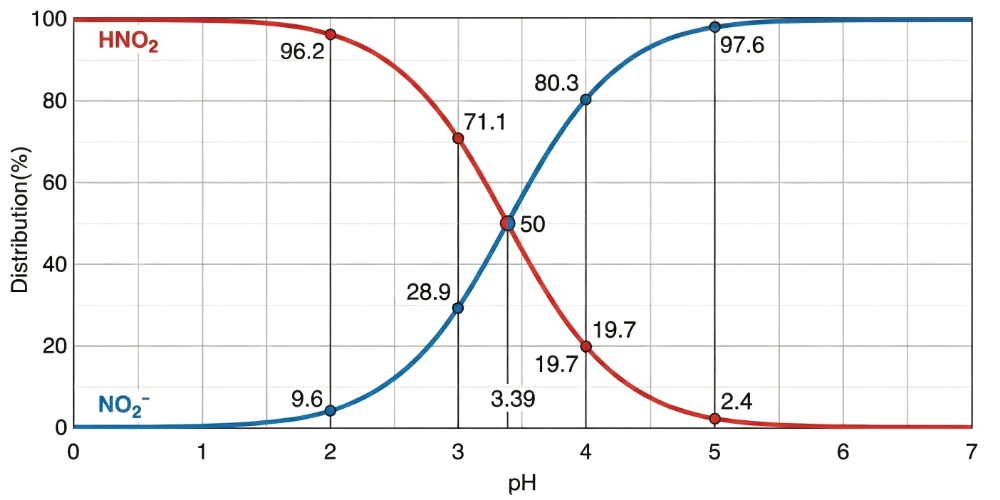
一般的な淡水~海水水槽(pH6~8.6)ではNO₂⁻が主体となります
グラフの通り、pHが7(中性)付近では、亜硝酸のほぼ100%が青い線の「亜硝酸イオン(NO₂⁻)」として存在しています。しかし、pHが下がり酸性に傾くにつれて、赤い線の「亜硝酸(HNO₂)」の割合が徐々に上昇し始めるのがわかります。
この現象は、特定の淡水環境において「見えない時限爆弾」となります。
ケース①:大型魚・カメ・両生類(古い水)
アロワナやオスカー、ミズガメなどは水を汚すスピードが速く、ろ過の過程でKH(炭酸塩硬度)を大量に消費します。水換えを怠って「古い水」になると、緩衝作用がなくなりpHが4〜5台まで急降下することがあります。
この状態で亜硝酸が発生すると、強毒のHNO₂が増え、特にウロコがないナマズの仲間や、皮膚から吸収する両生類、飼育水を飲む水生カメには致命的な環境になってしまいます。
ケース②:南米産水草・アピストグラマ(低pH低KH運用)
現地環境に合わせるため、意図的にpH5.0〜6.0付近、KHは0近くで管理する水槽です。
生体にとって理想的な環境ですが、一度ろ過バランスが崩れると、中性環境よりもはるかに毒性の強いHNO₂が発生するリスクと隣り合わせです。
また、硝化細菌の記事でも触れますがKHが0の環境では硝化バクテリアの炭素源が枯渇することで硝化が止まり、亜硝酸(HNO₂)が急速に増えることがあります。
亜硝酸の毒性メカニズム
では、アンモニアが分解された後に発生する「亜硝酸」には、具体的にどのような毒性があるのでしょうか?
アンモニアが「細胞破壊」や「神経毒」としての作用を持つのに対し、亜硝酸の毒性は主に「血液の酸素運搬を阻害することによる窒息(酸欠)」と、「強い酸化力による酵素や細胞の破壊」です。
ここでは、水槽内で問題となる3つの主な毒性メカニズムについて解説します。
亜硝酸の毒性①:魚類で起こるメトヘモグロビン血症(酸欠)
私たち人間と同じ脊椎動物である魚の血液(赤血球)には「ヘモグロビン」が含まれています。
ヘモグロビンの中心にある「鉄(Fe²⁺)」が酸素と結合することで、全身へ酸素を運搬しています。
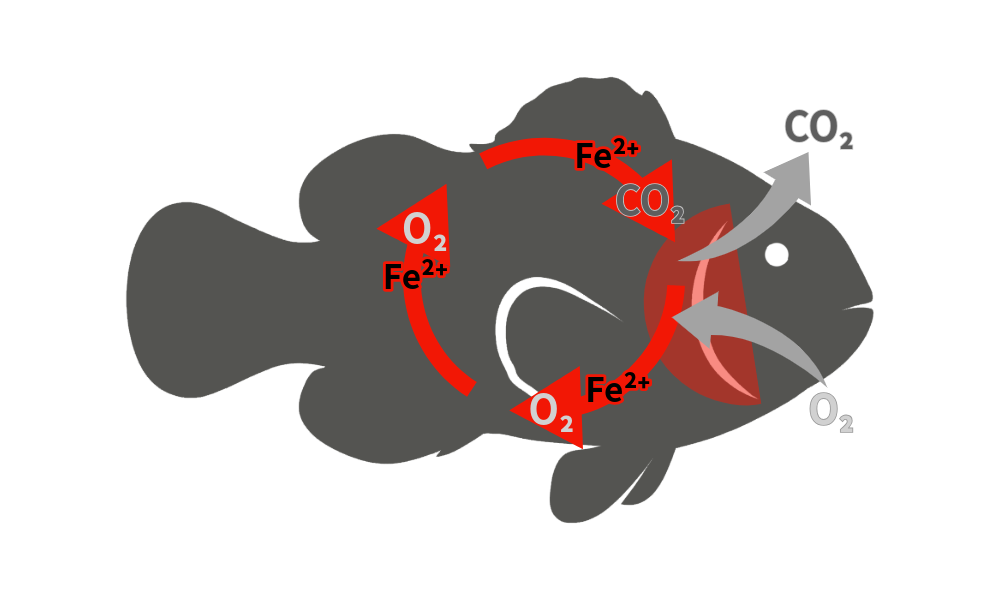
血液(赤血球)中のヘモグロビンが全身に酸素をおくります
しかし、体内に入った亜硝酸はこの鉄を酸化させ、酸素と結合できない「メトヘモグロビン(Fe³⁺)」へと変質させてしまいます。これを「メトヘモグロビン血症(ブラウン・ブラッド病)」と呼びます。
⚠️ ポイント
この病気にかかった魚は、エラが鮮やかな赤色から「茶褐色(チョコレート色)」に変色します。
・酸素と結びついたヘモグロビン=鮮やかな赤
・酸素が結びつけないメトヘモグロビン=茶褐色
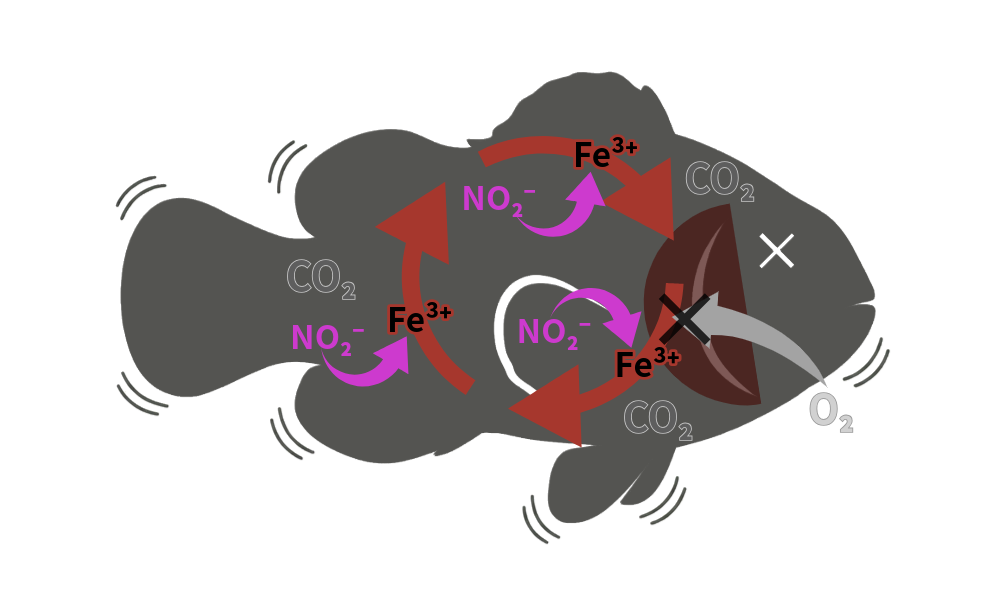
ヘモグロビンの核にある「Fe²⁺」が亜硝酸により「Fe³⁺」に変質し、酸素(O₂)を運べなくなります
この状態になると、いくら水槽内に酸素があっても血液が酸素を運べなくなり、二酸化炭素(CO₂)の排出効率も著しく下がるため、生体は内部から酸欠状態になり窒息死してしまいます。
亜硝酸の毒性②:甲殻類のヘモシアニン機能不全と脱皮不全
エビやカニなどの甲殻類、タコやイカなどの軟体動物は、血液中にヘモグロビンではなく、「銅(Cu)」を含む「ヘモシアニン」を持っています。亜硝酸は鉄だけではなく銅をも酸化(メトヘモシアニン化)させて酸素運搬能力を奪うため、魚同様に酸欠を引き起こします。
特に危険なのは、「酸素と結合していない状態のヘモシアニンほど、亜硝酸と反応しやすい」という点です。
つまり、水槽内の溶存酸素量が低下し、生体が酸欠気味である場合ほど、亜硝酸の毒性が加速度的に高まることを意味します。
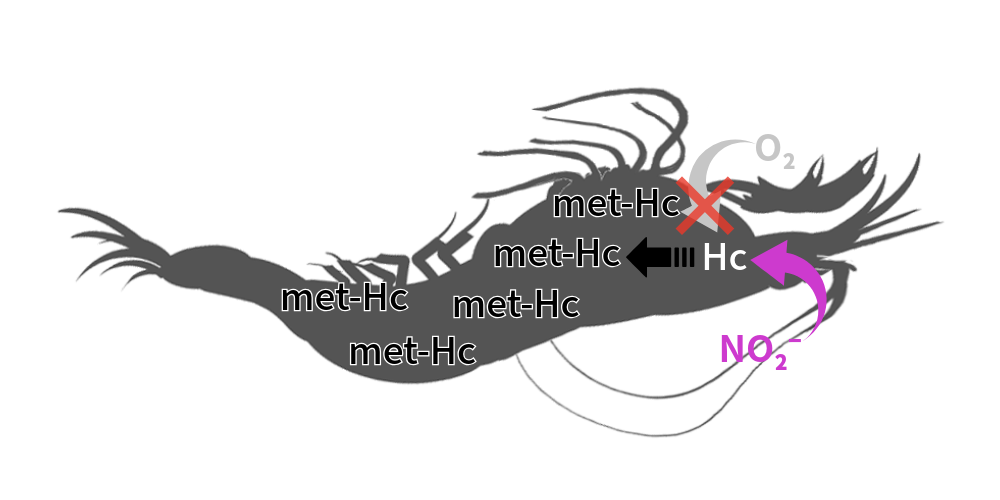
メトヘモシアニン(met-Hc)に変質してしまうことで酸欠になります
さらに、亜硝酸は甲殻類の成長に不可欠な「脱皮」を分子レベルで阻害します。
亜硝酸は生体組織を傷つける極めて強力な酸化力を持っているため、 細胞内に侵入すると、その激しい酸化ストレスが内分泌系を撹乱し、特に脱皮ホルモン受容体(EcR)の遺伝子発現を抑制してしまいます。
亜硝酸中毒が発生するときは同時にアンモニア中毒も併発する可能性が高いため、アンモニアによる浸透圧調整機能の異常も合わさって脱皮時の水分調整がうまくいかず、殻が脱げなくなって死んでしまうケースが多発します。
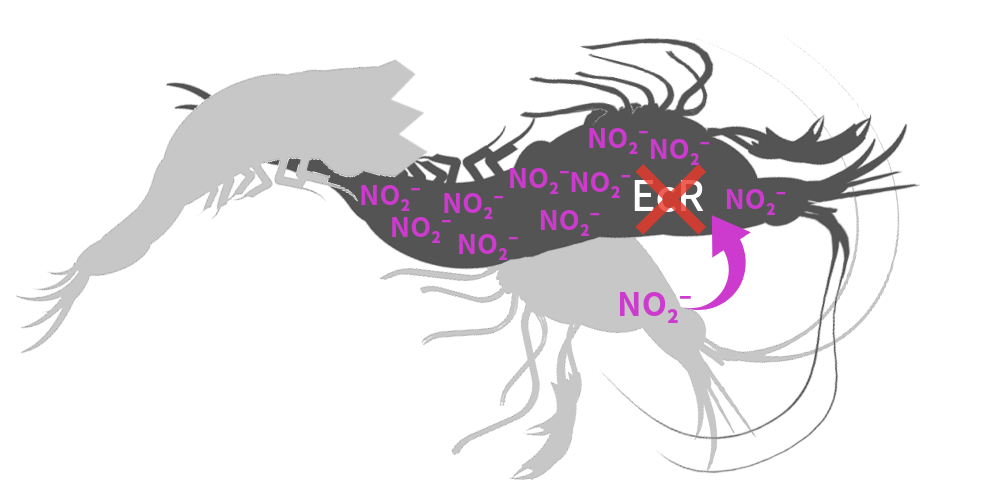
脱皮ホルモン受容体(EcR)が抑制され、正常な脱皮ができなくなります
シュリンプ水槽で「ポツポツ死」が止まらない場合、低濃度の亜硝酸が原因であることも少なくありません。
また、このホルモンの阻害作用は、脱皮以外でもさまざまな代謝に影響が現れます。
そのため、万が一亜硝酸中毒から生き延びても、繁殖率の低下や短命化のリスクが残ります。
亜硝酸の毒性③:光合成の阻害とサンゴの色落ち
窒素はサンゴと共生する褐虫藻の栄養源となりますが、過剰な亜硝酸は共生する褐虫藻の光合成システム(光化学系II)を阻害します。
光合成がスムーズに行われないと、利用されなかった光エネルギーが有害な活性酸素(ROS)へと変わり、サンゴの組織を内側から攻撃します。
さらにミトコンドリアの代謝系にも異常をきたし、色素の合成も阻害されてしまいます。
これによりサンゴの色素が破壊され、褐虫藻の色だけが目立つ「褐色化」を引き起こします。
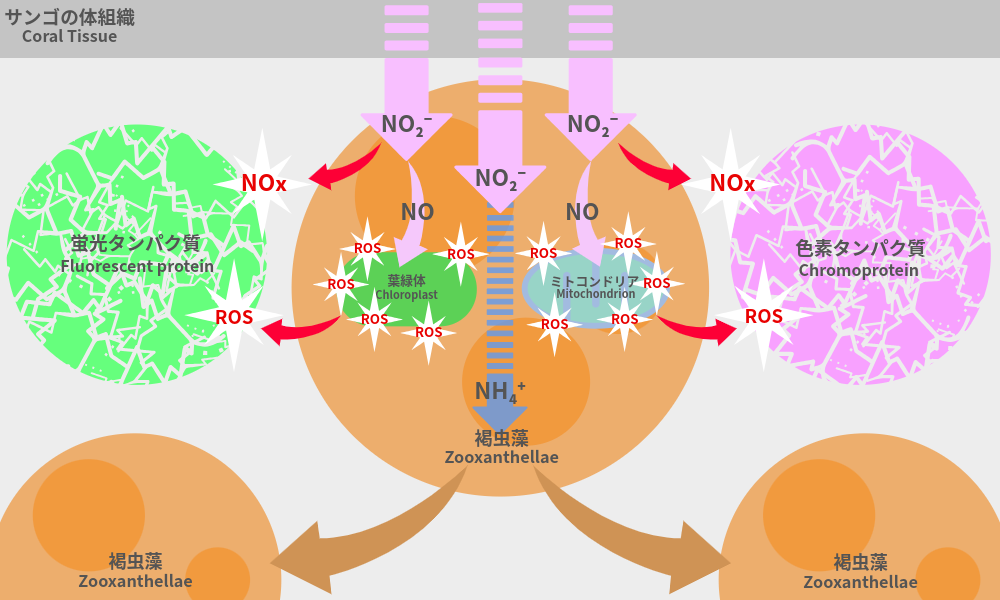
褐虫藻は窒素供給により増えますが、色素は酸化ストレスで破壊され、サンゴは褐色化します
さらに酸化ストレスが高まると、サンゴは防衛行動として褐虫藻を体外へ放出します。
これが「白化」の原因のひとつとなります。
サンゴや海藻、水草の光合成機能を健全に保つためには、亜硝酸が検出されない環境を維持する必要があります。
▼関連記事:サンゴの酸化ストレス耐性向上についてはこれらの記事をご覧ください。
淡水と海水における決定的な違い:塩分(塩化物イオン)のバリア
「海水魚水槽では、アンモニア中毒は聞くけれど、亜硝酸中毒で魚が全滅した話はあまり聞かない」 そう感じたことはありませんか?
実は、亜硝酸の毒性は、水中の「塩分(塩化物イオン)」の量によって劇的に変わります。
pH6以上の一般的な淡水水槽と海水水槽では亜硝酸はほとんどがイオン(NO₂⁻)の形をとります。
亜硝酸の形態は変わらないのに、淡水と海水で毒性が大きく変わるのは、塩分(塩化物イオン)の存在が大きく関わっているからです。
魚のエラにある「取り込み口」の競合
魚やエビのエラには、生命維持に必要な塩分(塩化物イオン:Cl⁻)を取り込むための専用の入り口があります。構造がよく似ている亜硝酸イオン(NO₂⁻)は、この取り込み口を「勘違い」させて、魚の体内に侵入します。
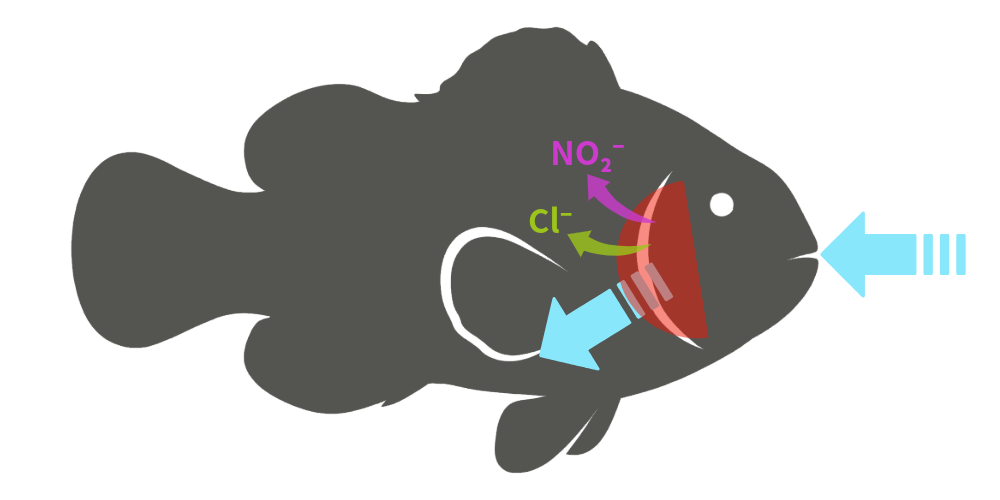
【海水の場合】塩化物イオンによるブロック
海水には、本来のターゲットである塩化物イオン(Cl⁻)が大量に含まれています。
そのため、取り込み口での「椅子取りゲーム」において塩化物イオンが圧倒的に有利となり、亜硝酸イオン(NO₂⁻)の侵入が物理的にブロックされます。
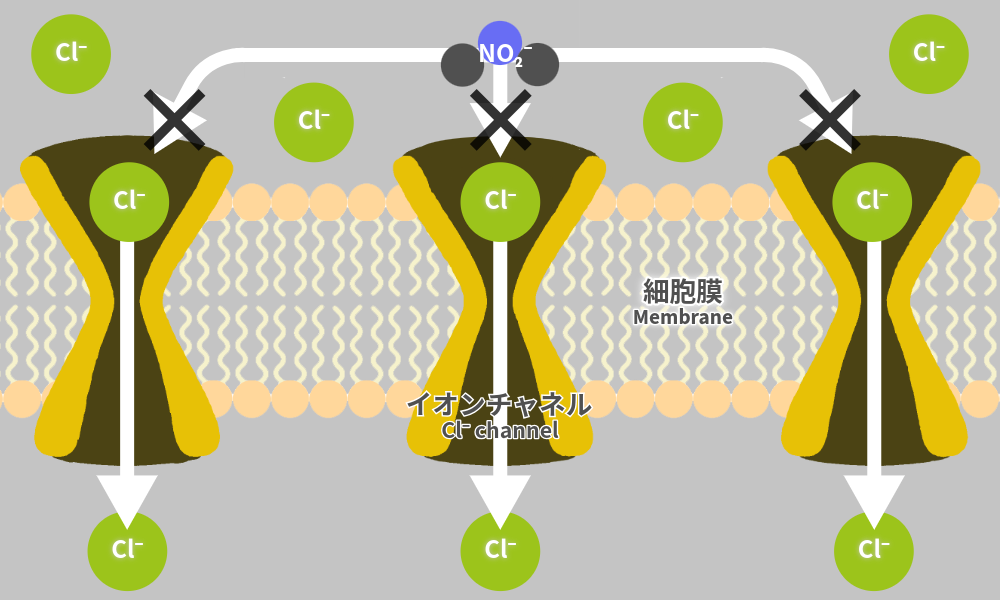
さらに、海水魚は周りが塩分だらけなので、エラを使って積極的に塩分を取り込む必要がありません。
そのため、淡水魚のような強力な取り込み装置は働いておらず、「イオンチャネル=イオンの通り道」から自然に入り込んでくるのを待つだけです。
このイオン取り込み方式を「受動拡散」といいます。
これに加え、前述した「水中に存在する大量の塩化物イオン(Cl⁻)によるブロック効果」が合わさるため、海水魚やが亜硝酸中毒になるリスクは極めて低くなります。
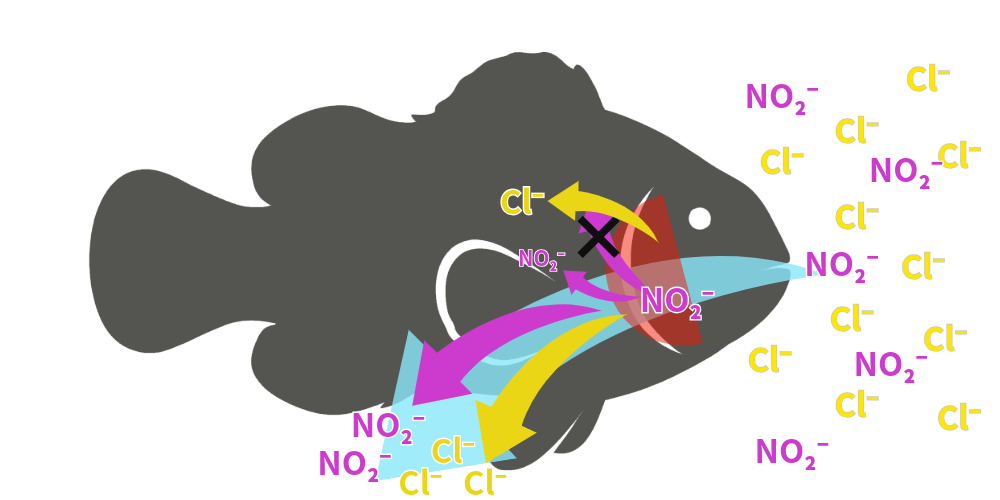
海水魚は受動拡散とCl⁻イオンによるブロック効果が合わさり、NO₂⁻の侵入は限定的になります
【海水魚の落とし穴】
「海水魚は亜硝酸に強いから安心」と油断してはいけません。
海水魚は、「アンモニア中毒」のリスクが淡水魚よりもはるかに高いという弱点があります。pHが高い海水中では毒性の強いアンモニア(NH₃)が発生しやすく、さらに海水から水分を得るため海水を大量に飲む習性があるため、消化管からも毒性の強いNH₃を吸収してしまいます。
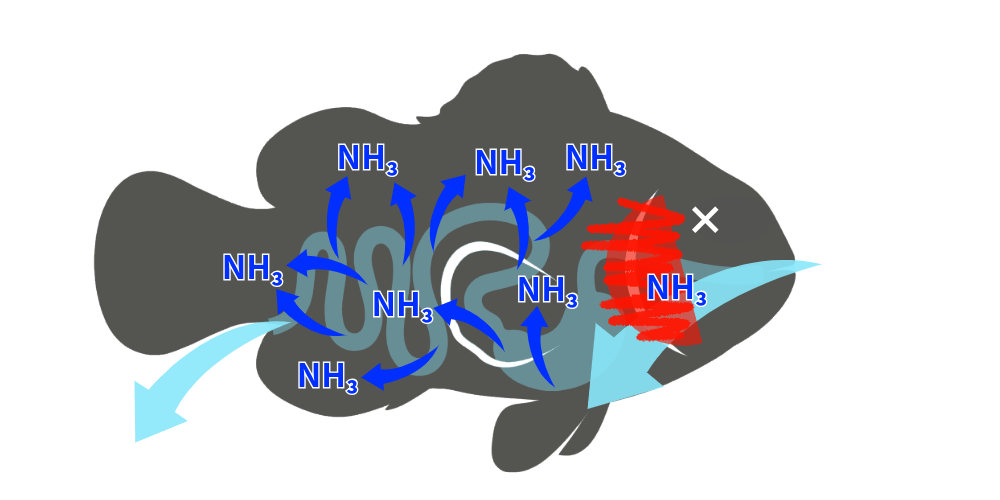
【海水と一緒にNH₃も取り込んでしまう海水魚のイメージ図】
海水魚はエラに加えて内臓にもNH₃のダメージを受けてしまいます結局のところ、淡水・海水を問わず、アンモニアと亜硝酸を無害化する「硝化バクテリア」の働きが生命線であることに変わりはありません。
【淡水の場合】無防備な侵入
一方、淡水にはNO₂⁻と競合する塩化物イオン(Cl⁻)がほとんど存在しません。
そのため、エラの取り込み口は防御のない「ガラ空き」の状態です。
また、淡水魚の体液は、周りの水よりも塩分濃度が高い状態にあります。
そのため、浸透圧の原理で常に体から塩分が水中に逃げ出そうとしています。
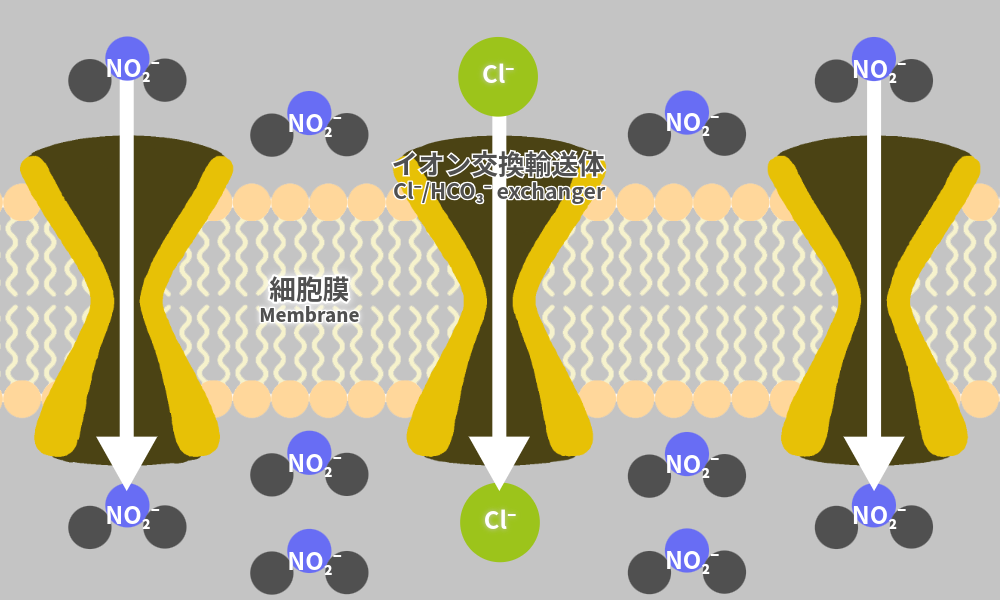
淡水魚は体内の塩分を維持するため、エラにある「イオン交換輸送体」をフル稼働させ、エネルギーを使って水中のわずかな塩分(Cl⁻)を自発的に取り込んでいます。
このイオン取り込み方式を「能動輸送」といいます。
自然な流入に留まる海水魚の「受動拡散」に対し、「能動輸送」は「ポンプのように強力な力でイオンを吸い上げる仕組み」になっています。この強力なポンプは、塩分(Cl⁻)だけでなく、形状の似た亜硝酸イオン(NO₂⁻)も区別なく強力に吸い込んでしまいます。
その結果、水中の亜硝酸濃度が低くても、淡水魚の血液中では水中の数十倍〜数百倍の濃度まで濃縮されてしまうのです。
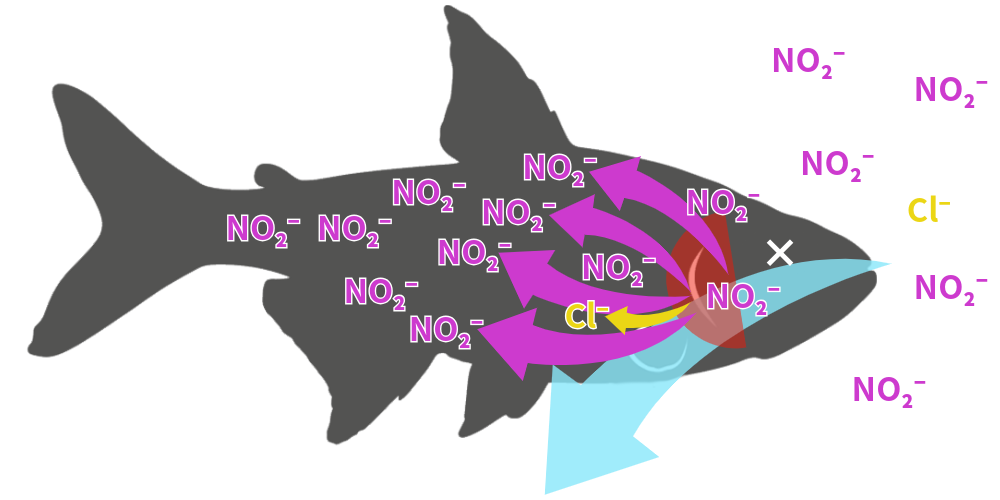
淡水魚は能動的にイオンを取り込むため、NO₂⁻も一緒に取り込み、体内で濃縮されてしまいます
この取り込みメカニズムの違いにより、同じサイズの金魚(淡水魚)とカクレクマノミ(海水魚)を比較した場合、金魚の方が圧倒的に大量の亜硝酸を取り込みます。
その差はわずかなものではなく、水産学の研究では亜硝酸の毒性への耐性に100倍以上もの開きがあることが示唆されています。
亜硝酸中毒が疑われるときの対処法
淡水魚は、その生理的な仕組みの違いから、海水魚に比べて亜硝酸中毒のリスクが格段に高いという特徴があります。もし水質検査薬で亜硝酸が検出された場合(0.2mg/L以上)、あるいは魚が水面で口をパクパクさせる「鼻上げ」をしている場合は、直ちに対処が必要です。
特に、魚のエラを確認できる場合、鮮やかな赤色ではなく「どす黒い茶色(チョコレート色)」に変色していたら、亜硝酸中毒の決定的なサインです。
基本的にはアンモニア中毒のときと近い処置となりますが、亜硝酸中毒は血液が酸素を運べなくなる「メトヘモグロビン血症」を引き起こすため、「酸欠対策」に重点を置いた応急処置を行います。
①大量の水換え、別容器への隔離(亜硝酸の希釈)

まずはアンモニア中毒と同様、まずは水中の亜硝酸総量を物理的に減らし、濃度を安全圏まで下げます。
緊急時は50%程度の水換えを行いますが、水温やpHのショックを与えないよう、新しい水は必ず水温とpHを合わせてから注水してください。
また、亜硝酸中毒の症状が重い場合は、別容器に隔離して治療を行う方が良い場合もあります。
【⚠️ 重要な注意点】
新しい水は、必ず「水温」と「pH」を元の水と合わせてください。
弱っている魚に急激な水質変化(pHショックや水温ショック)を与えると、それがトドメになってしまう危険があります。※pH合わせが難しい場合でも、最低限「水温」だけは必ず一致させましょう。
② エアレーションの強化(呼吸のサポート)

亜硝酸中毒への本命の対処法です。
メトヘモグロビン血症は、血中のヘモグロビンが変質して酸素を運べない状態になっています。
しかし、一瞬で全てのヘモグロビンがダメになってしまっているわけではありません。
魚が鼻上げをしている段階であれば、まだ助かる可能性があります。
通常よりも強めにエアレーションを行い、水中の酸素量をなるべく高めて呼吸を助けてあげてください。
また、魚には変質したヘモグロビンを元に戻す酵素(メトヘモグロビン還元酵素)が備わっています。
水中の亜硝酸を完全に断った状態で、魚が自力で回復するには通常24時間〜48時間ほどかかります。
その間、窒息しないよう 酸素を充分に供給し続けることが重要です。
| エアレーション期間 | 約24〜48時間 |
【⚠️ 重要な注意点】
エアレーションの勢いで魚が流されてしまうほどの強水流はNGです。
水流に逆らうために体力を消耗し、逆効果になります。
「水流は強くなりすぎず、充分な酸素を供給」できるよう、エアストーンなどを工夫してください。
③給餌の一時中断とバクテリア剤の投入

エサを与えると、魚の排泄物から新たなアンモニアが発生し、それが分解されてさらに亜硝酸濃度が上がってしまいます。亜硝酸濃度が上がるということは、毒性の強い亜硝酸を比較的無害な硝酸塩に変えるニトロバクタ―などの硝化バクテリアが充分に活動できていない状態にあります。
水中から亜硝酸をなくすためにはこれらのバクテリアがしっかり機能している状態にする必要があります。
極端に痩せてしまっている魚でなければ、数日〜1週間程度エサを食べなくても餓死することはありません。
まずは毒性の強い亜硝酸を消すことが最優先です。
また、硝化バクテリアは自然に増えますが、ある程度軌道に乗るまでは時間がかかります。
バクテリアの増殖期間を短縮させるために、硝化バクテリア剤を投入して様子を見ることも有効です。

硝化バクテリアが充分に増殖し、亜硝酸が検出されなくなれば給餌を再開しても大丈夫です。
④0.1%〜0.3%程度の塩水浴(淡水魚の場合)

亜硝酸中毒への最も安全かつ効果的な対策として、多くの研究で推奨されているのが「塩(塩化物イオン=Cl⁻)」の添加です。特に淡水魚においては特効薬といえるくらいに有効な手段となります。
これは、「亜硝酸が魚の体内に入り込むことを塩化物イオンがブロックする」という明確な防御メカニズムに基づいています。
メチレンブルーなどの魚病薬とは異なり、塩はろ過バクテリア(硝化バクテリア)への悪影響が少ないため、塩分に弱い生き物がいなければ本水槽に直接投入することもできます。
なお、亜硝酸中毒に使用する塩については、汽水魚や海水魚の飼育とは異なり、塩化物イオン(Cl⁻)によるNO₂⁻の取り込みブロックを目的としているため、一般的な食塩(塩化ナトリウム)でも問題ありません。
ただし、食用の塩ではアジシオなどのように、余分な調味料などが加えられているものがあるため注意しましょう。
| 推奨濃度 | 0.1%〜0.3%(水10Lに対して塩10g〜30g) |
| 使用する塩 | 一般的な「食塩(塩化ナトリウム)」でも問題ありません。 |
| 薬浴期間 | 本水槽の水から亜硝酸(NO₂⁻)が検出されなくなるまで。 |
| 使用する「塩」の目安 |
| 観賞魚用塩 ・人工海水 | ◎ 最適 | ミネラルバランスが調整されているものもあり、安心です。 |
| あら塩 (海塩・天然塩) | ○ 推奨 | 成分がほぼ「塩化ナトリウム」だけのもの。 岩塩などの天然塩の使用も問題ありません。 |
| 精製塩 (食卓塩) | △ 注意 | 「サラサラ」にするための固結防止剤が含まれている場合があります。緊急時以外は避けたほうが無難です。 |
| アジシオ (調理塩) | × 危険 | アミノ酸(うま味成分)や香辛料が含まれており、水質悪化や魚への害になります。絶対に使用しないでください。 |
【塩が⛔ 使用できないケース】
▶ナマズ類(コリドラス等)
ウロコを持たない魚は塩分に敏感なため、塩水浴は避け、隔離治療を推奨。
▶水草
一般的な水草は塩分に極めて弱いため、水草水槽には使用しないでください。
⑤亜硝酸中和剤・除去剤の投入(塩が使えない場合)
隔離水槽が用意できず、どうしても本水槽で治療しなければならない場合は、水換えを行った後に中和剤を使用しましょう。特に水草水槽など、後述する「塩」や「薬」が使えない環境では非常に有効な手段です。
現在(2026年2月時点)、日本国内で購入できる亜硝酸中和剤・除去剤は2種類あります。
シーケム「プライム」はカルキ抜きとして普段使いも可能なコンディショナーです。
セラ「トキシベック(アクアチューナー)」は亜硝酸を含むさまざまな有毒物質を無害化できるコンディショナーで、即効性が高いため緊急時にも使えるアイテムとなっています。
| シーケム「プライム」 |

| 特徴 | 亜硝酸を無害な形に結合・変換する。 |
| メリット | pHや酸素濃度への影響が少なく、常用しやすい。 |
| ⚠️ 注意点 | 一般的な試薬では無害化した亜硝酸の数値も検出される場合がある。 |
| セラ「トキシベック(アクアチューナー)」 |

| 特徴 | 有害物質を即座に分解・無害化する即効性タイプ。 |
| メリット | アンモニア・亜硝酸・クロラミン等をまとめて除去可能。 |
| ⚠️ 注意点 | 酸素を消費するため、必ずエアレーションを併用する。 |
| 推奨濃度 | 製品毎の規定量を厳守 |
| 薬浴期間 | 本水槽の水から亜硝酸(NO₂⁻)が検出されなくなるまで。 |
【⚠️ 重要な注意点】
これらの製品はあくまで「一時的な無害化」のためのものです。
根本的な解決にはろ過バクテリアの定着が必要ですので、継続的な水質チェックを怠らないでください。また、アンモニアの中和剤と同様に、亜硝酸の中和剤を使用し無害化した場合でも亜硝酸が検出されることがあります。中和剤を使用後に亜硝酸が検出されても焦らず、規定量以上の投入を行わないように注意してください。
⑥ メチレンブルーによる薬浴(最終手段・隔離必須)

亜硝酸中毒の症状が重篤な場合の最終的な切り札です。
魚病薬として一般的なメチレンブルーですが、白点病などの殺菌だけでなく、亜硝酸中毒によって酸素を運べなくなった血液を回復させる作用も持っています。
血液中に取り込まれたメチレンブルーは「電子の運び屋」として機能します。
酵素(NADPH)から受け取った電子をメトヘモグロビンへ渡し、還元により正常なヘモグロビンへ修復します。
この電子の受け渡しは一回きりではなく、メチレンブルーが血液中でこの働きを繰り返し、魚を酸欠状態から回復する手助けをします。
| 推奨濃度 | 1〜10 mg/L |
| 薬浴期間 | 約24〜48時間 |
【⚠️ 重要な注意点】
メチレンブルーは治療効果が高い反面、「硝化バクテリアを死滅させる」という重大なリスクがあります。本水槽に直接投与すると、生物ろ過が崩壊し、さらに亜硝酸濃度が上昇する悪循環に陥る危険性があります。
※軽度の場合や隔離が難しい場合は、ろ過バクテリアへの影響が少ない「中和剤の使用(③)」もしくは「塩水浴(④)」が第一選択として推奨されます。状況に応じて使い分けましょう。
▼参考文献
Lewis, W. M., & Morris, D. P. (1986). Toxicity of nitrite to fish: A review.
Kroupova, H., Machova, J., & Svobodova, Z. (2005). Nitrite influence on fish: a review.
亜硝酸中毒の予後について
アンモニア中毒と同様に亜硝酸中毒についても、これらの処置を行ったからといって、必ずしも全ての生体が助かるわけではありません。
人間においても酸欠は脳に重大なダメージを与え、ある一線を超えると不可逆的な(元に戻らない)ダメージとなります。 一度破壊された脳神経組織は、きれいな水に戻したからといって即座に再生するものではありません。
また、弱った生体が水換え後に死亡してしまうことがありますが、これは単純に水換えのショックだけではなく、「処置をした時点で、すでに致死的なダメージを負っていた(手遅れになっていた)」ケースも少なくありません。
助かったとしても脳神経にダメージが出てしまった場合、その後も泳ぎ方に異常が出るなど後遺症が残る可能性があります。
緊急時の対応を予め準備しておくことも大切ですが、それ以上に普段からアンモニア中毒や亜硝酸中毒が発生しないような安全な環境づくりが重要です。
まとめ
亜硝酸は、目に見えないところで生体の酸素を奪う恐ろしい毒です。
| 亜硝酸の毒性 |
| ▶毒性の正体: ・血液中のヘモグロビンを変質させ、「酸欠」を引き起こす(メトヘモグロビン血症)。 ・強い酸化力で酵素や体組織にダメージを与える ▶淡水水槽での影響: 能動的に濃縮してしまうため、ごく微量でも危険。 ▶海水水槽での影響:生理機能とイオン競合により毒性は抑制されるが、無脊椎動物への影響は大きい。 |
それぞれの環境におけるメカニズムを正しく理解し、適切なろ過システムの構築と定期的な水質検査で、大切な魚を酸欠のリスクから守ってあげてください。
次回は、これら危険なアンモニアや亜硝酸を無害化してくれる水槽の守護者「硝化バクテリア(ろ過バクテリア)」の解説です。
コメント